| Спиропентан | |
|---|---|
 | |
| Общие | |
| Хим. формула | C5H8 |
| Термические свойства | |
| Температура | |
| • плавления | −134,6 °C[1] |
| Классификация | |
| Рег. номер CAS | 157-40-4 |
| PubChem | 9088 |
| SMILES | |
| InChI | |
| ChemSpider | 8734 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Спиропента́н (спиро[2.2]пентан) — углеводород с химической формулой C5H8, содержащий в своей структуре два спиросочлененных (соединенных через один общий атом углерода) циклопропановых фрагмента. Спиропентан является простейшим алициклическим соединением спиранового ряда.[2][3][4][5]
После открытия спиропентана в 1887 году прошло несколько лет, прежде чем была определена структура молекулы.[6][7][8]
Согласно правилам номенклатуры ИЮПАК для спиросоединений,[9][10] систематическое название спиропентана — спиро[2.2]пентан. Однако у спиропентана не может быть других структурных изомеров, поэтому название, как правило, указывается без скобок и цифр.
История открытия
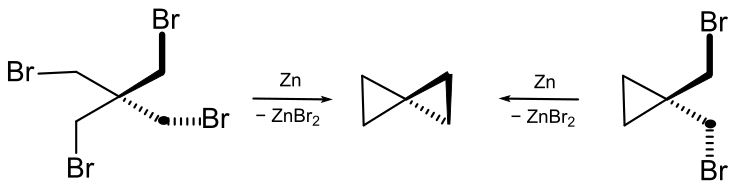
После того, как Гавриил Густавсон получил циклопропан путем взаимодействия 1,3-дибромпропана с измельченным цинком,
он провел аналогичную реакцию с 2,2-ди(бромметил)-1,3-дибромпропаном, который может быть получен реакцией пентаэритрита с бромоводородной кислотой. В результате реакции элиминирования было получено соединение состава C5H8, для которого изначально была предложена структура метиленциклобутана (винилтриметилена). [11] В 1907 году Фехт высказал предположение о том, что полученный в ходе этой реакции углеводород содержит два трехчленных цикла, соединенных через один общий атом углерода,[12] и, таким образом, отосится к классу спиросоединений, ранее описанных в работе фон Байера.[13] Правильность этого предположения была далее подтверждена Зелинским, который получил спиропентан встречным синтезом из 1,1-ди(бромметил)циклопропана:[14]
Спиропентан трудно отделить от побочных продуктов реакции (2-метил-1-бутена, 1,1-диметилциклопропана, метиленциклобутана), поэтому первые попытки его получения приводили к получению смесей продуктов. Позднее чистый спиропентан был выделен методом перегонки.[15]
Строение
Структурный анализ с помощью дифракции электронов показал в спиропентане различие длины C—C-связей: связи с четвертичным («спиро») атомом углерода короче (146,9 пм), чем между метиленовыми группами (CH2–CH2, 151,9 пм).
Углы C–C–C при спироатоме C составляют 62,2°, что больше, чем в циклопропане.[16]
Химические свойства
При нагревании молекул спиропентана, меченных атомами дейтерия, наблюдается реакция топомеризации или «стереомутации», аналогичная реакции циклопропана: цис-1,2-дидейтериоспиропентан находится в равновесии транс-1,2-дидейтериоспиропентаном.[17]
Густавсон в 1896 году сообщил, что нагрев спиропентана до 200 °C приводит к его превращению в другие углеводороды. Термолиз спиропентана в газовой фазе от 360 до 410°C ведет к его перегруппировке с расширеним цикла в структурный изомер - метиленциклобутан; побочно происходит образование продуктов фрагментации - этена и пропадиена.[18] Предположительно, в процессе перегруппировки в метиленциклобутан более длинная и более слабая связь между метиленовыми фрагментами спиропентана разрывается первой, образуя бирадикальный интермедиат.[17]
Примечания
- ↑ SPIROPENTANE (англ.) — 2007.
- ↑ Donohue, Jerry (1945). "The Structure of Spiropentane". Journal of the American Chemical Society. 67 (2): 332—335. doi:10.1021/ja01218a056. ISSN 0002-7863.
- ↑ Murray, M. J. (1944). "SPIROPENTANE". Journal of the American Chemical Society. 66 (2): 314. doi:10.1021/ja01230a515. ISSN 0002-7863.
- ↑ Murray, M. J. (1944). "The Debromination of Pentaerythrityl Bromide by Zinc. Isolation of Spiropentane1". Journal of the American Chemical Society. 66 (5): 812—816. doi:10.1021/ja01233a047. ISSN 0002-7863.
- ↑ Price, J.E. (2011). "High-resolution infrared spectra of spiropentane, C5H8". Journal of Molecular Spectroscopy. 269 (1): 129—136. doi:10.1016/j.jms.2011.05.011. ISSN 0022-2852.
- ↑ Philipow, O. (1916). "Die Konstitution der Kohlenwasserstoffe Gustavsons: Vinyltrimethylen und Äthylidentrimethylen". Journal für Praktische Chemie. 93 (1): 162—182. doi:10.1002/prac.19160930112. ISSN 0021-8383. Архивировано 29 июня 2021. Дата обращения: 29 июня 2021.
- ↑ Faworsky, Al. (1914). "Über das Vinyltrimethylen und Äthyliden-trimethylen von Gustavson". Berichte der Deutschen Chemischen Gesellschaft. 47 (2): 1648—1651. doi:10.1002/cber.19140470250. ISSN 0365-9496. Архивировано 29 июня 2021. Дата обращения: 29 июня 2021.
- ↑ Burns, G. R. (1972). "Infrared and Raman Spectra of Spiropentane-H8". Applied Spectroscopy. 26 (5): 540—542. doi:10.1366/000370272774351778.
- ↑ Определение спиросоединений по ИЮПАК (англ.). IUPAC - Spiro Compounds. Дата обращения: 13 февраля 2022. Архивировано 3 марта 2016 года.
- ↑ G.P. Moss. Extension and Revision of the Nomenclature for Spiro Compounds (англ.) // Pure Appl. Chem. : журнал. — 1999. — Vol. 71, no. 3. — P. 531—558. — ISSN 1365—3075. Архивировано 1 мая 2021 года.
- ↑ Gustavson, G. (1896). "Ueber Aethylidentrimethylen". Journal für Praktische Chemie. 54 (1): 104—107. doi:10.1002/prac.18960540106. ISSN 0021-8383. Архивировано 29 июня 2021. Дата обращения: 29 июня 2021.
- ↑ Fecht, H. (1907). "Über Spirocyclane". Berichte der Deutschen Chemischen Gesellschaft. 40 (3): 3883—3891. doi:10.1002/cber.190704003194. ISSN 0365-9496. Архивировано 29 июня 2021. Дата обращения: 29 июня 2021.
- ↑ Adolf Baeyer. Systematik und Nomenclatur bicyclischer Kohlenwasserstoffe (англ.) // Berichte der deutschen chemischen Gesellschaft. — 1900-10. — Vol. 33, iss. 3. — P. 3771–3775. — ISSN 0365-9496. — doi:10.1002/cber.190003303187.
- ↑ Zelinsky, N. (1913). "Über das Spirocyclan, seine Synthese und sein Verhalten bei der Reduktionskatalyse". Berichte der Deutschen Chemischen Gesellschaft. 46 (1): 160—172. doi:10.1002/cber.19130460128. ISSN 0365-9496. Архивировано 29 июня 2021. Дата обращения: 29 июня 2021.
- ↑ Applequist, Douglas E. (1958). "Chemistry of Spiropentane. I. An Improved Synthesis of Spiropentane". The Journal of Organic Chemistry. 23 (11): 1715—1716. doi:10.1021/jo01105a037. ISSN 0022-3263.
- ↑ G. Dallinga, R. K. van der Draai, L. H. Toneman, Recueil des Travaux Chimiques des Pays-Bas 87, 897 (1968).
- ↑ 1 2 J. J. Gajewski, L. T. Burka, Journal of the American Chemical Society 94, Nr. 25, 8857 (1972).
- ↑ M. C. Flowers, H. M. Frey, Journal of the Chemical Society, 1961, 5550.
Обычно почти сразу, изредка в течении часа.