| Майтотоксин | |
|---|---|
 | |
| Общие | |
| Традиционные названия | майтотоксин |
| Хим. формула | C164H256Na2O68S2 |
| Физические свойства | |
| Молярная масса | 3423,88336 г/моль |
| Термические свойства | |
| Температура | |
| • кипения | различная °C |
| Классификация | |
| Рег. номер CAS | 59392-53-9 |
| PubChem | 71460273 |
| Рег. номер EINECS | 800-521-0 |
| InChI | |
| ChemSpider | 25991548 |
| Безопасность | |
| Токсичность | черезвычайно ядовит, сильнейший органический яд |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
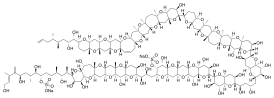
Майтотоксин — токсин небелковой природы, продуцируемый динофлагеллятами вида Gambierdiscus toxicus. Является одним из самых токсичных веществ, обнаруженных в живой природе, и, одновременно, одним из самых сложных по структуре веществ природного происхождения.
Майтотоксин чрезвычайно токсичен (доза в 130 нг/кг массы тела, при внутрибрюшинном введении, летальна для мышей)[1] и обладает, вероятно, самым сложным строением из всех известных небелковых веществ природного происхождения (правильность установления структуры и пространственного строения молекулы майтотоксина и в настоящее время вызывает сомнения, а попытки осуществить его полный синтез, начатые ещё в середине 1990-х годов, до сих пор не увенчались успехом).
История открытия и изучения
Изначально майтотоксин был выделен из рыб вида Ctenochaetus striatus (полосатый хирург), обитающих в экосистемах коралловых рифов и питающихся планктоном (биоаккумуляция токсина в организме некоторых видов хищных рыб (барракуды, морской окунь, мурены, сибас и др.), питающихся полосатым хирургом, приводит к отравлению людей, употребляющих рыбу этих видов в пищу). На Таити этот вид рыб известен как «maito», что и дало название этому токсину[2][3].
Структура и пространственное строение молекулы майтотоксина были установлены к середине 1990-х годов с использованием методов аналитической химии (масс-спектрометрия и двумерная спектроскопия ЯМР с предварительной частичной окислительной деградацией молекулы данного токсина). Но сомнения относительно правильности установления пространственного строения майтотоксина остаются до сих пор[4].
Необычность и сложность структуры (в том числе наличие в молекулах множества хиральных центров) таких соединений как майтотоксин, палитоксин и др. делают установление их строения само по себе очень сложной задачей и требуют привлечения усилий как наиболее компетентных учёных, так и использования самых передовых методов химического и физико-химического анализа (в том числе таких, которые ранее просто не существовали)[4]. Особую сложность представляет установление стереохимии (пространственного строения) подобных соединений. Даже само по себе получение достаточных количеств таких веществ является непростой задачей. Единственный доступный источник получения — выделение из живых организмов, которые осуществляют биосинтез либо биоаккумулируют их в себе (причём, как правило, содержание их очень невелико). К примеру, для получения в чистом виде майтотоксина пришлось на протяжении года культивировать динофлагеллят вида Gambierdiscus toxicus для получения около 4000 литров культуры (с концентрацией клеток 2⋅106/л), а затем применить многостадийный процесс выделения, концентрирования и очистки этого соединения. В итоге удалось получить порядка 5 мг химически чистого майтотоксина[4].
Работы над осуществлением полного синтеза майтотоксина были начаты в 1996 году и продолжаются (с перерывами) по настоящее время под руководством Кирьякоса Николау. Возглавляемые им группы учёных пока что смогли осуществить синтез некоторых отдельных частей, из которых состоит молекула майтотоксина[5][6][7][8][2].
Молекула майтотоксина состоит из 32 конденсированных колец, содержит 28 гидроксильных и 22 метильные группы, а также 2 эфира серной кислоты. Кроме того, в ней есть 98 хиральных центров. Всё это делает задачу по выполнению полного химического синтеза майтотоксина исключительно сложной.
Токсичность
LD50 — 50 нг/кг массы тела (для мышей), что делает майтотоксин наиболее токсичным из всех известных веществ небелковой природы.
Физиологическое действие майтотоксина состоит в нарушении гомеостаза внутриклеточного содержания Ca2+. Резкое повышение содержания ионов Са2+ внутри клеток, в конечном счёте, приводит к их гибели. Точный молекулярный механизм действия майтотоксина неизвестен, но предполагается, что он связывается с Ca-АТФазой, превращая её в ионный канал, через который ионы Ca2+ начинают неконтролируемо поступать во внутриклеточное пространство[9][10][11][12]
Примечания
- ↑ Akihiro Yokoyama, Michio Murata, Yasukatsu Oshima, Takashi Iwashita, Takeshi Yasumoto. Some Chemical Properties of Maitotoxin, a Putative Calcium Channel Agonist Isolated from a MarineDinoflagellate (англ.) // The Journal of Biochemistry. — 1988-08-01. — Vol. 104, iss. 2. — P. 184–187. — ISSN 0021-924X. — doi:10.1093/oxfordjournals.jbchem.a122438.
- ↑ 1 2 Katrina Krämer2018-03-09T14:28:00+00:00. Maitotoxin (англ.). Chemistry World. Дата обращения: 7 декабря 2019. Архивировано 7 декабря 2019 года.
- ↑ Ю.А. Владимиров. Биоорганическая химия. — Москва: Просвещение, 1987. — С. 772. — 815 с.
- ↑ 1 2 3 В.А. Стоник, И.В. Стоник. Морские токсины: химические и биологические аспекты изучения (рус.) // Успехи химии : журнал. — 2010. — Т. 79, № 5. — С. 451—452.
- ↑ K. C. Nicolaou, Kevin P. Cole, Michael O. Frederick, Robert J. Aversa, Ross M. Denton. Chemical Synthesis of the GHIJK Ring System and Further Experimental Support for the Originally Assigned Structure of Maitotoxin // Angewandte Chemie International Edition. — 2007. — Т. 46, вып. 46. — С. 8875–8879. — ISSN 1521-3773. — doi:10.1002/anie.200703742. Архивировано 7 декабря 2019 года.
- ↑ K. C. Nicolaou, Michael O. Frederick, Antonio C. B. Burtoloso, Ross M. Denton, Fatima Rivas. Chemical Synthesis of the GHIJKLMNO Ring System of Maitotoxin // Journal of the American Chemical Society. — 2008-06-01. — Т. 130, вып. 23. — С. 7466–7476. — ISSN 0002-7863. — doi:10.1021/ja801139f.
- ↑ K. C. Nicolaou, Robert J. Aversa, Jian Jin, Fatima Rivas. Synthesis of the ABCDEFG Ring System of Maitotoxin // Journal of the American Chemical Society. — 2010-05-19. — Т. 132, вып. 19. — С. 6855–6861. — ISSN 0002-7863. — doi:10.1021/ja102260q.
- ↑ K. C. Nicolaou, Philipp Heretsch, Tsuyoshi Nakamura, Anna Rudo, Michio Murata. Synthesis and Biological Evaluation of QRSTUVWXYZA′ Domains of Maitotoxin // Journal of the American Chemical Society. — 2014-11-19. — Т. 136, вып. 46. — С. 16444–16451. — ISSN 0002-7863. — doi:10.1021/ja509829e.
- ↑ Yasushi Ohizumi, Takeshi Yasumoto. Contraction and increase in tissue calcium content induced by maitotoxin, the most potent known marine toxin, in intestinal smooth muscle (англ.) // British Journal of Pharmacology. — 1983. — Vol. 79, iss. 1. — P. 3–5. — ISSN 1476-5381. — doi:10.1111/j.1476-5381.1983.tb10485.x.
- ↑ William G. Sinkins, Mark Estacion, Vikram Prasad, Monu Goel, Gary E. Shull. Maitotoxin converts the plasmalemmal Ca2+ pump into a Ca2+-permeable nonselective cation channel // American Journal of Physiology-Cell Physiology. — 2009-09-30. — Т. 297, вып. 6. — С. C1533–C1543. — ISSN 0363-6143. — doi:10.1152/ajpcell.00252.2009. Архивировано 8 декабря 2019 года.
- ↑ Mark Estacion, William P. Schilling. Maitotoxin-induced membrane blebbing and cell death in bovine aortic endothelial cells // BMC Physiology. — 2001-02-06. — Т. 1, вып. 1. — С. 2. — ISSN 1472-6793. — doi:10.1186/1472-6793-1-2.
- ↑ Kevin K. W. Wang, Rathna Nath, Kadee J. Raser, Iradj Hajimohammadreza. Maitotoxin Induces Calpain Activation in SH-SY5Y Neuroblastoma Cells and Cerebrocortical Cultures // Archives of Biochemistry and Biophysics. — 1996-07-15. — Т. 331, вып. 2. — С. 208–214. — ISSN 0003-9861. — doi:10.1006/abbi.1996.0300.
Обычно почти сразу, изредка в течении часа.
