| Ионол | |
|---|---|
 | |
| Общие | |
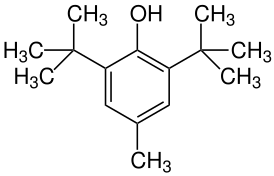
| Систематическое наименование |
2,6-ди-трет-бутил-4-метил-фенол |
| Сокращения | BHT |
| Традиционные названия | Ионол, бутилгидрокситолуол, дибунол, агидол-1, 2,6-ди-трет-бутил-п-крезол |
| Хим. формула | C15H24O |
| Физические свойства | |
| Молярная масса | 220,35 г/моль |
| Плотность | 1,048 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 69-73 °C |
| • кипения | 265 °C |
| • вспышки | 261 ± 1 ℉[1] |
| Давление пара | 0,01 ± 0,01 мм рт.ст.[1] |
| Классификация | |
| Рег. номер CAS | 128-37-0 |
| PubChem | 31404 |
| Рег. номер EINECS | 204-881-4 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E321 |
| RTECS | GO7875000 |
| ChEBI | 34247 |
| ChemSpider | 13835296 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Ионол, бутилгидрокситолуол, дибунол, агидол-1, BHT — 2,6-дитретбутил-4-метилфенол, липофильное органическое вещество, представитель класса фенолов, широко использующееся в химической промышленности в качестве антиоксиданта.
Получение
Ионол получают по реакции Фриделя — Крафтса алкилированием п-крезола изобутиленом[2]:
Также может быть получен алкилированием в отсутствие кислотных катализаторов[3].
Свойства и применение
Технический ионол — порошок жёлтого цвета, в чистом виде — белый порошок[3]. Применяется в качестве антиоксиданта в производстве пищевых продуктов (пищевая добавка E321), смазочных масел, каучуков, пластмасс и др. Также является исходным соединением для синтеза различных производных пространственно затруднённых фенолов, многие из которых обладают биологической активностью или находят применение в промышленности. Хорошо растворяется в изопентане, бензоле, спирте, ацетоне, сложных эфирах, жирах. Нерастворим в воде и 10%-м растворе едкого натра[4].
Механизм действия
По химическим свойствам ионол является синтетическим аналогом витамина E, подавляя автокаталитические процессы радикального окисления[5]. Ионол является донором атома водорода, превращая пероксидные радикалы в гидропероксиды[6]:
где R — алкильная или арильная группа, ArOH — ионол или аналогичный фенольный антиоксидант, P — нерадикальные и неактивные продукты окисления фенола.
Каждая молекула ионола деактивирует две молекулы пероксидных радикалов[5].
Безопасность
Ведутся дебаты о связи ионола с риском развития рака[7]. Некоторые исследования показывают повышение, а некоторые — понижение риска[8][9][10]. Поступление в организм малых доз ионола и бутилированого гидроксианизола (BHA) с пищей может иметь положительный эффект, защищая от вредных веществ[11][12].
В медицине
Благодаря возможности нейтрализовывать свободные радикалы и прерывать цепные реакции с участием свободных радикалов, 5%-й линимент дибунола широко применялся в качестве наружнего противоожогового и противовоспалительного средства. Дибунол также успешно применялся для лечения некоторых видов рака, лучевых и трофических поражений кожи и слизистых оболочек и т. д.[13] В настоящее время не выпускается.
Ионол также является компонентом ректальных суппозиториев.
См. также
Примечания
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0246.html
- ↑ Fiege H., Voges H.-W., Hamamoto T., Umemura S., Iwata T., Miki H., Fujita Y., Buysch H.-J., Garbe D., Paulus W. Phenol Derivatives // Ullmann's Encyclopedia of Industrial Chemistry. — Wiley, 2000. — doi:10.1002/14356007.a19_313.
- ↑ 1 2 Ершов В. В., Никифоров Г. А., Володькин А. А. Пространственно-затрудненные фенолы. — М.: Химия, 1972. — 352 с.
- ↑ Харлампович Г. Д., Чуркин Ю. В. Фенолы. — М.: Химия, 1974. — С. 19—20. — 376 с. — 3300 экз.
- ↑ 1 2 Burton G. W., Ingold K. U. Autoxidation of biological molecules. 1. Antioxidant activity of vitamin E and related chain-breaking phenolic antioxidants in vitro // J. Am. Chem. Soc.. — 1981. — Т. 103, вып. 21. — С. 6472—6477. — doi:10.1021/ja00411a035.
- ↑ Денисов Е. Т. Лекция 14. МЕХАНИЗМ ДЕЙСТВИЯ АНТИОКСИДАНТОВ. Дата обращения: 19 января 2014. Архивировано 9 января 2014 года.
- ↑ Butylated hydroxytoluene (BHT) (англ.) // IARC Monographs on the Evaluation of Carcinogenic Risks to Humans. — 1986. — Vol. 40. — P. 161—206.
- ↑ Kensler T. W., Egner P. A., Trush M. A., Bueding E., Groopman J. D. Modification of aflatoxin B1 binding to DNA in vivo in rats fed phenolic antioxidants, ethoxyquin and a dithiothione (англ.) // Carcinogenesis. — 1985. — Vol. 6, no. 5. — P. 759—763. — doi:10.1093/carcin/6.5.759.
- ↑ Williams G.M., Iatropoulos M. J. Inhibition of the hepatocarcinogenicity of aflatoxin B1 in rats by low levels of the phenolic antioxidants butylated hydroxyanisole and butylated hydroxytoluene (англ.) // Cancer Lett.. — 1996. — Vol. 104, iss. 1. — P. 49—53.
- ↑ Franklin R. A. Butylated hydroxytoluene in sarcoma-prone dogs (англ.) // Lancet. — 1976. — Vol. 1, iss. 7972. — P. 1296.
- ↑ Grice H. C., Clayson D. B., Flamm W. G., Ito N., Kroes R., Newberne P. M., Scheuplein R. Possible mechanisms of BHA carcinogenicity from a consideration of its chemical and biological properties (англ.) // Food and Chemical Toxicology. — 1986. — Vol. 24, iss. 10-11. — P. 1235—1242. — doi:10.1016/0278-6915(86)90312-1.
- ↑ Botterweck A. A. M., Verhagen H., Goldbohm R. A., Kleinjans J., P.A van den Brandt. Intake of butylated hydroxyanisole and butylated hydroxytoluene and stomach cancer risk: results from analyses in the Netherlands Cohort Study // Food and Chemical Toxicology. — 2000. — Т. 38, вып. 7. — С. 599—605. — doi:10.1016/S0278-6915(00)00042-9.
- ↑ Эмануэль Н.М. Кинетика экспериментальных опухолевых процессов. — М.: Наука, 1977. — 416 с.
Обычно почти сразу, изредка в течении часа.




