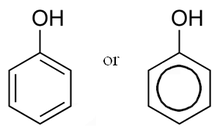
Фено́лы — органические соединения ароматического ряда, в молекулах которых гидроксильные группы OH− связаны с атомами углерода ароматического кольца.
Классификация
По числу ароматических ядер (бензольных колец) различают собственно фенолы (1 бензольное кольцо), нафтолы (2 кольца), антролы (3 кольца), фенантролы (4 кольца), бензотетролы (5 колец).
По числу ОН-групп различают:
- одноатомные фенолы (аренолы): фенол (C6H5OH) и его гомологи;
- двухатомные фенолы (арендиолы): пирокатехин, резорцин, гидрохинон (соответственно 1,2-, 1,3- и 1,4-дигидроксибензолы);
- трёхатомные фенолы (арентриолы): пирогаллол, гидроксигидрохинон, флороглюцин (соответственно 1,2,3-, 1,2,4- и 1,3,5-тригидроксибензолы),
- многоатомные фенолы
Изомерия
Возможны 2 типа изомерии:
- изомерия положения заместителей в бензольном кольце;
- изомерия боковой цепи (строения алкильного радикала и числа радикалов).
Электронное строение
Фенолы представляют собой полярные соединения (диполи). Бензольное кольцо является отрицательным концом диполя, а OH-группа — положительным. Дипольный момент направлен в сторону бензольного кольца.

Как известно, гидроксильная группа -OH является заместителем I рода, то есть она способствует повышению электронной плотности в бензольном кольце (особенно в орто- и пара-положениях). Это обусловлено тем, что одна из неподелённых пар электронов атома кислорода OH-группы вступает в сопряжение с π-системой бензольного кольца. Смещение неподелённой пары электронов атома кислорода в сторону бензольного кольца приводит к увеличению полярности связи O—H. Таким образом, имеет место взаимное влияние атомов и атомных групп в молекуле фенола. Это взаимное влияние отражается в свойствах фенола[1].
Во-первых, повышается способность к замещению атомов водорода в орто- и пара-положениях бензольного ядра, и в результате реакций замещения обычно образуются три-замещённые производные фенола.
Во-вторых, увеличение полярности связи O—H под действием бензольного ядра и появление достаточно большого положительного заряда на атоме водорода приводит к тому, что молекулы фенола диссоциируют в водных растворах по кислотному типу.
Фенол является слабой кислотой. В этом состоит главное отличие фенолов от спиртов, которые являются неэлектролитами.
Физические свойства
Большинство одноатомных фенолов при нормальных условиях представляют собой бесцветные кристаллические вещества с невысокой температурой плавления и характерным запахом. Фенолы малорастворимы в воде, хорошо растворяются в органических растворителях, токсичны, при хранении на воздухе постепенно темнеют в результате окисления. Фенол C6H5OH (карболовая кислота) — бесцветное кристаллическое вещество, на воздухе окисляется и становится розовым, при обычной температуре ограниченно растворим в воде, выше 66 °C смешивается с водой в любых соотношениях. Фенол — токсичное вещество, вызывает ожоги кожи, является антисептиком.
В живых организмах
Фенол представляет собой окончание боковой группы стандартной аминокислоты тирозина, и поэтому входит в состав практически каждой белковой молекулы[2].
Химические свойства
1. Реакции с участием гидроксильной группы
Кислотные свойства
- Диссоциация в водных растворах с образованием фенолят-ионов и ионов водорода;
- Взаимодействие со щелочами с образованием фенолятов (отличие от спиртов);
- Взаимодействие с активными металлами с образованием фенолятов (образующиеся в результате реакций 2 и 3) феноляты легко разлагаются при действии кислот. Даже такая слабая кислота, как угольная, вытесняет фенол из фенолятов, следовательно, фенол — ещё более слабая кислота, чем угольная).
При взаимодействии фенолятов с галогенпроизводными образуются простые и сложные эфиры.
2. Реакции с участием бензольного кольца
Реакции замещения
- Галогенирование (взаимодействие с галогенами)
- Нитрование (взаимодействие с азотной кислотой)
- Сульфирование (взаимодействие с серной кислотой)
Реакции присоединения
- Гидрирование (восстановление водородом до циклогексанола)
Качественные реакции на фенолы
В водных растворах одноатомные фенолы взаимодействуют с хлоридом железа(III) с образованием комплексных фенолятов, которые имеют фиолетовую окраску; окраска исчезает после прибавления синильной кислоты
Способы получения
1. Из каменноугольной смолы. Каменноугольную смолу, содержащую в качестве одного из компонентов фенол, обрабатывают вначале раствором щёлочи (образуются феноляты), а затем — кислотой.
2. Сплавление аренсульфокислот со щёлочью: C6H5-SO3Na + NaOH → C6H5-OH + Na2SO3
3. Взаимодействие галогенпроизводных ароматических углеводородов со щелочами: C6H5-Cl + NaOH → C6H5-OH + NaCl
или с водяным паром: C6H5-Cl + H2O → C6H5-OH + HCl
Применение фенолов
Фенолы широко применяются в производстве пластмасс, резин, лекарств, моющих средств, ядохимикатов, топлива и других веществ. Основное применение фенолы находят в производстве различных феноло-альдегидных смол, полиамидов, полиарилатов, полиариленсульфонов, поликарбонатов, эпоксидных смол, антиоксидантов, бактерицидов и пестицидов (например, нитрафен). Алкилфенолы используют в производстве ПАВ, стабилизаторов и присадок к топливам. Двухатомные фенолы и их производные входят в состав дубителей для кожи и меха, модификаторов и стабилизаторов резин и каучуков, применяются для обработки кино- и фотоматериалов. В медицине фенолы и их производные используют в качестве антимикробных (фенол, резорцин), противовоспалительных (салол, осарсол), спазмолитических (адреналин, папаверин), жаропонижающих (аспирин, салициловая кислота), слабительных (фенолфталеин), адреномиметических (мезатон), вяжущих (танины) и других лекарственных средств, а также витаминов E и P.
Примечания
Литература
Синович А. Д., Павлов Г. П. Фенолы // Химическая энциклопедия : в 5 т. / Гл. ред. Н. С. Зефиров. — М.: Большая Российская энциклопедия, 1998. — Т. 5: Триптофан — Ятрохимия. — 783 с. — 10 000 экз. — ISBN 5-85270-310-9.
Ссылки
Обычно почти сразу, изредка в течении часа.
