Сорбция (от лат. sorbeo — поглощаю) — поглощение твёрдым телом либо жидкостью различных веществ из окружающей среды. Поглощаемое вещество, находящееся в среде, называют сорбатом (сорбтивом), поглощающее твёрдое тело или жидкость — сорбентом.
По характеру поглощения сорбата сорбционные явления делятся на два типа: адсорбцию — концентрирование сорбата на поверхности раздела фаз или его поглощение поверхностным слоем сорбента и абсорбцию — объёмное поглощение, при котором сорбат распределяется по всему объёму сорбента.
В свою очередь, различают два типа адсорбции — физическую адсорбцию, при которой повышение концентрации сорбата на поверхности раздела фаз обусловлено неспецифическими (то есть не зависящими от природы вещества) силами Ван-дер-Ваальса и химическую адсорбцию (хемосорбцию), обусловленную протеканием химических реакций сорбата с веществом поверхности сорбента. Физическая адсорбция слабоспецифична, обратима и её тепловой эффект невелик (единицы к Дж/моль). Хемосорбция избирательна, обычно необратима и её теплота составляет от десятков до сотен (хемосорбция кислорода на металлах) к Дж/моль.
В вакуумной технике явление сорбции используют титановые насосы.
Энциклопедичный YouTube
-
1/3Просмотров:12 0142 16116 212
-
Адсорбция. Учебный фильм по химии
-
Сорбция платиновых металлов ферроцианидами
-
Sorption: A Close-Up View
Субтитры
Абсорбция
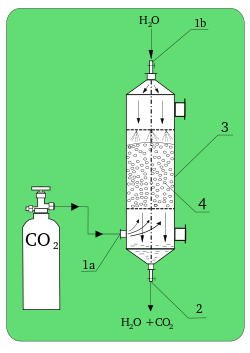
Абсорбция в химии — физический или химический феномен или процесс, при котором атомы, молекулы или ионы входят в какое-либо объёмное состояние — газ, жидкость или твёрдое тело. Это процесс, отличный от адсорбции, поскольку молекулы, подвергающиеся абсорбции, забираются по объёму, а не по поверхности (как происходит в случае с адсорбцией). Более общий термин — сорбция, который охватывает процессы абсорбции, адсорбции и ионного обмена. Абсорбция, в основном — это процесс, при котором что-то присоединяет другую субстанцию.[1]
Если абсорбция является физическим процессом, не сопровождаемым другими физическими или химическими процессами, она обычно подчиняется закону распределения Нернста:
- "при равновесии отношение концентраций третьего компонента в двух жидких состояниях является постоянной величиной.";
Объём постоянной KN зависит от температуры и называется коэффициентом распределения. Это равенство верно при условии, что концентрации не слишком велики и если молекулы "х" не меняют свою форму в любом другом из двух состояний. Если такая молекула подвергается ассоциации или диссоциации, тогда это равенство всё так же описывает равновесие между "х" в обоих состояниях, но только для той же формы — концентрации всех оставшихся форм должны быть рассчитаны с учетом всех остальных равновесий.[1]
В случае газовой абсорбции можно рассчитать концентрацию используя например Закон идеального газа, c = p/RT. В качестве альтернативы можно использовать парциальное давление вместо концентраций.
Во многих технологически важных процессах, химическая абсорбция используется вместо физического процесса, например абсорбция углекислого газа гидроксидом натрия — такие процессы не следуют закону распределения Нернста.
Для некоторых примеров этого эффекта можно рассмотреть экстракцию, при которой можно извлечь компонент из одной жидкой фазы раствора и перенести в другую без химической реакции. Примеры таких растворов — благородные газы и оксид осмия.[1]
Ссылки
- ↑ 1 2 3 McMurry, John. Fundamentals of Organic Chemistry (неопр.). — Fifth. — Agnus McDonald, 2003. — С. 409. — ISBN 0534395732.
Обычно почти сразу, изредка в течении часа.

![{\displaystyle {\frac {[x]_{1}}{[x]_{2}}}={\text{constant}}=K_{N(x,12)}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e0ec1ce71d0ce27734b33e4d1dfae04be91ecf13)