Биосинтез холестерина — образование в живом организме органического спирта холестерина стероидной природы. Синтез холестерина происходит в клетках печени (50 %), кишечнике и коже. В клетке он идёт в гладком эндоплазматическом ретикулуме и цитозоле. Биосинтез холестерина служит основой синтеза других стероидных соединений. Начальные этапы синтеза являются общими с этапами синтеза других изопреноидов.

В 1940-е годы Блох с сотр. установил, что все атомы углерода холестерина происходят из ацетата, причём оба атома включаются в одинаковых количествах. В настоящее время установлена следующая цепь биосинтеза холестерина, включающая в себя несколько ступеней. (Образование промежуточных соединений этого пути может происходить и другими способами).
- Превращение трёх молекул активного ацетата в пятиуглеродный мевалонат.
- Превращение мевалоната в активный изопреноид — изопентенилпирофосфат.
- Образование тридцатиуглеродного изопреноида сквалена из шести молекул изопентенилдифосфата.
- Циклизация сквалена в ланостерин.
- Последующее превращение ланостерина в холестерин.
Синтез мевалоната
Синтез мевалоната протекает в три этапа.
- Образование ацетоацетил-КоА из двух молекул ацетил-КоА с помощью тиолазного фермента ацетоацетилтрансферазы. Реакция обратима. Происходит в цитозоле.
- Образование β-гидрокси-β-метилглутарил-КоА из ацетоацетил-коА с третьей молекулой ацетил-КоА с помощью гидроксиметилглутарил-КоА-синтазы (ГМГ-КоА-синтазы). Реакция также обратима. Происходит в цитозоле.
- Образование мевалоната восстановлением ГМГ и отщеплением HS-KoA с помощью НАДФ-зависимой гидроксиметилглутарил-КоА-редуктазы (ГМГ-КоА-редуктаза). Происходит в гЭПР. Это первая практически необратимая реакция в цепи биосинтеза холестерина, а также она лимитирует скорость биосинтеза холестерина. Отмечены суточные колебания синтеза этого фермента. Активность его увеличивается при введении инсулина и тиреоидных гормонов, снижается при голодании, введении глюкагона, глюкокортикоидов.
Существуют и другие пути синтеза мевалоната.
Синтез изопентенилпирофосфата
- 1, 2. Вначале мевалоновая кислота дважды фосфорилируется с помощью АТФ: до 5-фосфомевалоната, а затем до 5-пирофосфомевалоната.
- 3. 5-пирофосфомевалонат фосфорилируется по 3 атому углерода, образуя нестабильный промежуточный продукт — 3-фосфо-5-пирофосфомевалонат.
- 4. Последний декарбоксилируется и дефосфорилируется, образуется изопентенилпирофосфат.
Синтез сквалена
- Изопентенилпирофосфат изомеризуется в диметилаллилпирофосфат.
- Конденсация изопентенилпирофосфата (С5) с диметилаллилпирофосфатом (С5) и образование геранилпирофосфата (С10). При этом высвобождается молекула пирофосфата.
- Конденсация изопентенилпирофосфата (С5) с геранилпирофосфатом (С10). Образуется фарнезилпирофосфат (С15) и высвобождается ещё одна молекула пирофосфата.
- Конденсация двух молекул фарнезилпирофосфата (С15) «голова-к-голове» и образование сквалена (С30). Реакция проходит с затратой НАДФН, и высвобождаются две молекулы пирофосфата. Молекулы фарнезилпирофосфата конденсируются концами, несущими пирофосфатные группы. Сначала отщепляется одна пирофосфатная группа и образуется промежуточный прескваленпирофосфат. Он, в свою очередь, восстанавливается с помощью НАДФН. Второй пирофосфат уходит. Образуется сквален.
Начиная со сквалена, продукты пути биосинтеза холестерина нерастворимы в водной среде и участвуют в дальнейших реакциях, будучи связанными со стеринпереносящими белками (СПБ).
Синтез ланостерина
- 1. Под действием скваленэпоксидазы образуется эпоксид сквалена.
- 2. Затем эпоксид сквалена циклизуется в ланостерин. При этом метильная группа у С14 переносится на С13, а метильная группа у С8 — на С14.
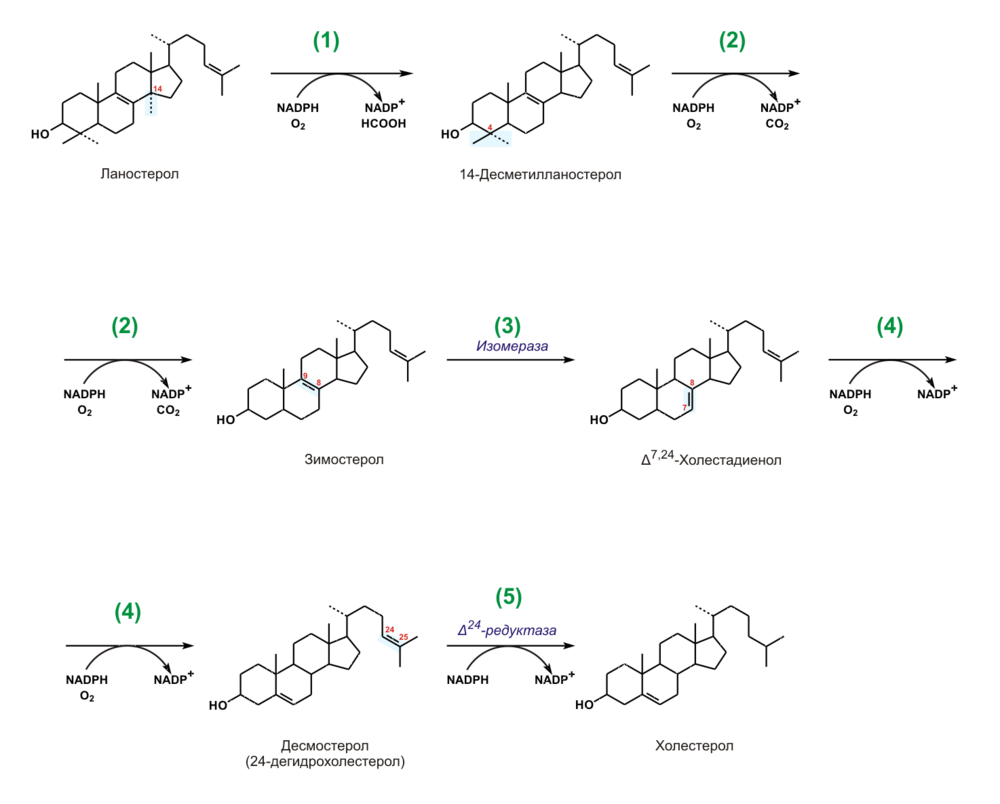
Синтез холестерина
Ланостерин превращается в мембранах гладкого эндоплазматического ретикулума в холестерин.
- Метильная группа при С14 окисляется, и образуется 14-десметилланостерин.
- 2. Затем удаляются ещё два метила при С4, и образуется зимостерол.
- 3. Далее двойная связь C8=С9 перемещается в положение С8=С7 и образуется Δ7,24-холестадиенол.
- 4. Двойная связь далее перемещается в положение С5=С6,образуется десмостерол.
- 5. После чего в боковой цепи восстанавливается двойная связь, и образуется холестерин.
(Восстановление двойной связи в боковой цепи может, однако, происходить и на предшествующих стадиях биосинтеза холестерола.)
Другие пути синтеза
У некоторых организмов при синтезе стероидов могут встречаться другие варианты реакций (например, немевалонатный путь образования пятиуглеродных молекул).
Литература
- [www.xumuk.ru/biologhim/169.html Химическая энциклопедия сайта www.humuk.ru. Скан учебника «Биологическая химия», Берёзов Т. Т., Коровкин Б. Ф.]
- Кольман Я., Рём К.-Г., «Наглядная биохимия», пер. с нем., М., «Мир», 2009.
- Марри Р., Греннер Д., Мейес П., Родуэлл В., «Биохимия человека». М., «Мир», 1993.
Обычно почти сразу, изредка в течении часа.





