
La quiralidad es una propiedad de asimetría importante en varias ramas de la ciencia. La palabra quiralidad proviene del griego χειρ (kheir), ‘mano’, un objeto quiral familiar.
Un objeto o un sistema es quiral si es distinguible de su imagen reflejada; es decir, no puede superponerse sobre ella. A la inversa, una imagen de espejo de un objeto aquiral, como una esfera, no se puede distinguir del objeto. Un objeto quiral y su imagen especular se denominan enantiomorfos (griego, ‘formas opuestas’) o, cuando se refieren a moléculas, enantiómeros. Un objeto no quiral se llama aquiral (a veces también anfíceo) y se puede superponer en su imagen de espejo. Si el objeto no es quiral y se imagina que es de color azul y su imagen reflejada se imagina como de color amarillo, entonces, mediante una serie de rotaciones y traslaciones, las dos pueden superponerse, produciendo verde, sin que quede ninguno de los colores originales.
El término fue usado por primera vez por Lord Kelvin en 1893 en la segunda Conferencia de Robert Boyle en el Club Científico Juvenil de la Universidad de Oxford, que se publicó en 1894:
Llamo "quiral" a cualquier figura geométrica, o grupo de puntos, y digo que tiene quiralidad si su imagen en un espejo plano, idealmente realizada, no puede coincidir con ella misma.William Thomson Lord Kelvin[1]
Las manos humanas son quizás el ejemplo de quiralidad más reconocido universalmente. La mano izquierda es una imagen de espejo no superponible de la mano derecha; no importa cómo estén orientadas las dos manos, es imposible que todas las características principales de ambas manos coincidan en todos los ejes.[2] Esta diferencia en la simetría se hace evidente si alguien intenta estrechar la mano derecha de una persona con la mano izquierda o si se coloca un guante zurdo en la mano derecha. En matemáticas, la quiralidad es la propiedad de una figura que no es idéntica a su imagen reflejada.
YouTube Encyclopedic
-
1/3Views:18 09015 83113 030
-
Introducción a la quiralidad
-
Ejemplos quirales 1
-
quiralidad
Transcription
Matemáticas


En matemáticas, una figura es quiral (y se dice que tiene quiralidad) si no puede asignarse a su imagen reflejada mediante rotaciones y traslaciones solamente. Por ejemplo, un zapato derecho es diferente de un zapato izquierdo, y en el sentido de las agujas del reloj es diferente de un zapato derecho. Ver[3] para una definición matemática completa.
Un objeto quiral y su imagen reflejada se dice que son enantiomorfos. La palabra enantiomorfo proviene del griego ἐναντίος (enantíos) ‘enfrente’, y μορφή (morfé) ‘forma’. Una figura no quiral se llama aquiral o anfichiral.
La hélice (y, por extensión, una cuerda hilada, un tornillo, una hélice, etc.) y la tira de Möbius son objetos quirales de dos dimensiones en un espacio ambiental tridimensional. Los tetrominos en forma de J, L, S y Z del popular videojuego Tetris también presentan quiralidad, pero solo en un espacio bidimensional.
Muchos otros objetos familiares exhiben la misma simetría quiral del cuerpo humano, como guantes, gafas (donde dos lentes difieren en la receta) y zapatos. Una noción similar de quiralidad se considera en la teoría de nudos, como se explica a continuación.
A algunos objetos tridimensionales quirales, como la hélice, se les puede asignar una orientación diestra o zurda, de acuerdo con la regla de la mano derecha.
Geometría
En geometría, una figura es aquiral si y solo si su grupo de simetría contiene al menos una isometría de inversión de orientación. En dos dimensiones, cada figura que posee un eje de simetría es aquiral, y se puede demostrar que cada figura achiral acotada debe tener un eje de simetría. En tres dimensiones, cada figura que posee un plano de simetría o un centro de simetría es aquiral. Sin embargo, hay figuras aquirales que carecen de plano y centro de simetría. En términos de grupos de puntos, todas las figuras quirales carecen de un eje de rotación inadecuado (Sn). Esto significa que no pueden contener un centro de inversión (i) o un plano de espejo (σ). Solo las cifras con una designación de grupo de puntos de C1, Cn, Dn, T, O o I pueden ser quirales.
Teoría de nudos
Un nudo se llama aquiral si puede deformarse continuamente en su imagen de espejo, de lo contrario se llama quiral. Por ejemplo, el nudillo y el nudo en forma de ocho son aquirales, mientras que el nudo trébol es quiral.
Física
En física, la quiralidad se puede encontrar en el giro de una partícula, donde la habilidad del objeto está determinada por la dirección en que gira la partícula.[4] No debe confundirse con la helicidad, que es la proyección del giro a lo largo del momento lineal de una partícula subatómica, la quiralidad es un fenómeno puramente cuántico mecánico como el giro. Aunque ambos pueden tener propiedades para zurdos o diestros, solo en el caso sin masa tienen una relación simple.[5] En particular, para una partícula sin masa, la helicidad es la misma que la quiralidad, mientras que para una antipartícula tienen un signo opuesto.
La habilidad tanto en la quiralidad como en la helicidad se relaciona con la rotación de una partícula mientras se realiza en movimiento lineal con referencia a las manos humanas. El pulgar de la mano apunta hacia la dirección del movimiento lineal, mientras que los dedos se doblan hacia la palma, representando la dirección de rotación de la partícula (es decir, en el sentido de las agujas del reloj y en el sentido contrario a las agujas del reloj). Dependiendo del movimiento lineal y de rotación, la partícula puede definirse por la mano izquierda (por ejemplo, la traducción hacia la izquierda y la rotación hacia la izquierda) o por la mano derecha (por ejemplo, la traducción en la dirección correcta y la rotación hacia la derecha).[5] Una transformación de simetría entre los dos se llama paridad. La invariancia bajo paridad por un fermión de Dirac se llama simetría quiral.
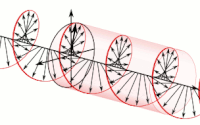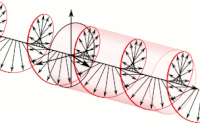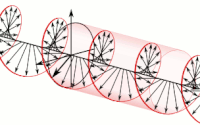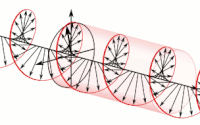
Electromagnetismo
La propagación de la onda electromagnética, en la medida en que se transmite, es polarización de la onda y se describe en términos de helicidad (ocurre como una hélice). La polarización de una onda electromagnética es la propiedad que describe la orientación, es decir, la variación en el tiempo, la dirección (vector) y la amplitud del vector del campo eléctrico. Para una representación, vea la imagen adyacente.
Química

Una molécula quiral es un tipo de molécula que tiene una imagen especular no superponible. La característica que más a menudo es la causa de la quiralidad en las moléculas es la presencia de un átomo de carbono asimétrico.[6][7]
El término "quiral" en general se usa para describir el objeto que no se puede superponer en su imagen de espejo.[8]
En química, la quiralidad generalmente se refiere a las moléculas. Dos imágenes especulares de una molécula quiral se denominan enantiómeros o isómeros ópticos. Los pares de enantiómeros se designan a menudo como "diestro", "zurdo" o, si no tienen sesgo, "aquiral". A medida que la luz polarizada pasa a través de una molécula quiral, el plano de polarización, cuando se ve a lo largo del eje hacia la fuente, se girará en el sentido de las agujas del reloj (hacia la derecha) o en el sentido contrario a las agujas del reloj (hacia la izquierda). Una rotación hacia la derecha es dextrorotaria (d); que a la izquierda es levorotaria (l). Los isómeros d y l son el mismo compuesto, pero se denominan enantiómeros. Una mezcla equimolar de los dos isómeros ópticos no producirá una rotación neta de la luz polarizada a medida que pasa.[9] Las moléculas zurdas tienen prefijo a sus nombres; d- es el prefijo de moléculas diestras.
La quiralidad molecular es de interés debido a su aplicación a la estereoquímica en química inorgánica, química orgánica, química física, bioquímica y química supramolecular.
Los desarrollos más recientes en química quiral incluyen el desarrollo de nanopartículas inorgánicas quirales que pueden tener una geometría tetraédrica similar a los centros quirales asociados con los átomos de carbono sp3 tradicionalmente asociados con compuestos quirales, pero a mayor escala.[10][11] También se obtuvieron simetrías helicoidales y otras de nanomateriales quirales.[12]
Biología
Todas las formas de vida conocidas muestran propiedades quirales específicas en estructuras químicas, así como anatomía macroscópica, desarrollo y comportamiento.[13] En cualquier organismo específico o conjunto relacionado evolutivamente del mismo, los compuestos individuales, órganos o comportamiento se encuentran en la misma forma enantiomórfica única. La desviación (que tiene la forma opuesta) se puede encontrar en una pequeña cantidad de compuestos químicos, o en ciertos órganos o comportamientos, pero esa variación depende estrictamente de la composición genética del organismo. Desde el nivel químico (escala molecular), los sistemas biológicos muestran una estereoespecificidad extrema en la síntesis, la captación, la detección y el procesamiento metabólico. Un sistema vivo usualmente trata con dos enantiómeros de un mismo compuesto de una manera drásticamente diferente.
En biología, la homoquiralidad es una propiedad común de los aminoácidos y carbohidratos. Los aminoácidos que producen proteínas quirales, que se traducen a través del ribosoma a partir de la codificación genética, se presentan en forma de L. Sin embargo, los D- aminoácidos también se encuentran en la naturaleza. Los monosacáridos (unidades de carbohidratos) se encuentran comúnmente en la configuración D. La doble hélice del ADN es quiral (como cualquier tipo de hélice es quiral), y la forma B del ADN muestra un giro hacia la derecha.
A veces, cuando dos enantiómeros de un compuesto se encuentran en los organismos, difieren significativamente en su sabor, olor y otras acciones biológicas. Por ejemplo, (+) - limoneno encontrado en naranja (causando su olor), y (-) - limoneno encontrado en limones (causando su olor), muestra diferentes olores[14] debido a diferentes interacciones bioquímicas en la nariz humana. (+) - Carvone es responsable del olor del aceite de semilla de alcaravea, mientras que (-) - carvone es responsable del olor del aceite de menta verde.[15]

Además, para los compuestos artificiales, incluidos los medicamentos, en el caso de los medicamentos quirales, los dos enantiómeros a veces muestran una diferencia notable en el efecto de sus acciones biológicas.[16] Darvon (dextropropoxifeno) es un analgésico, mientras que su enantiómero, Novrad (levopropoxifeno) es un agente contra la tos. En el caso de la penicilamina, el (isómero S utilizado en el tratamiento de la artritis crónica primaria, mientras que el isómero (R) no tiene ningún efecto terapéutico y es muy tóxico.[17] En algunos casos, el enantiómero menos activo terapéuticamente puede causar efectos secundarios. Por ejemplo, ( S- naproxeno es un analgésico, pero el isómero R causa problemas renales.[18] La forma natural de la planta de alfa-tocoferol (vitamina E) es RRR-α-tocoferol, mientras que la forma sintética (vitamina E racémica, o dl-tocoferol) es parte igual de los estereoisómeros RRR, RRS, RSS, SSS, RSR, SRS, SRR y SSR con equivalencia biológica que disminuye progresivamente, de modo que 1.36 mg de dl-tocoferol se considera equivalente a 1.0 mg de d-tocoferol.[19]

Ejemplos macroscópicos de quiralidad se encuentran en el reino vegetal, el reino animal y todos los otros grupos de organismos. Un ejemplo simple es la dirección de enrollamiento de cualquier planta trepadora, que puede crecer para formar una hélice de zurdos o zurdos.

En anatomía, la quiralidad se encuentra en la simetría imperfecta de la imagen de espejo de muchos tipos de cuerpos animales. Los organismos como los gasterópodos exhiben quiralidad en sus envolturas enrolladas, lo que resulta en una apariencia asimétrica. Más del 90% de las especies de gasterópodos[20] tienen conchas dextrales (diestras) en su enrollamiento, pero una pequeña minoría de especies y géneros son casi siempre sinistrales (zurdos). Muy pocas especies (por ejemplo, Amphidromus perversus[21]) muestran una mezcla igual de individuos dextrales y sinistrales.
En los seres humanos, la quiralidad (también conocida como mano de obra o lateralidad ) es un atributo de los humanos definido por su distribución desigual de la habilidad motora fina entre las manos izquierda y derecha. Un individuo que es más diestro con la mano derecha se llama diestro, y el que es más hábil con la izquierda se dice que es zurdo. La quiralidad también se observa en el estudio de la asimetría facial.
En los peces planos, la platija es de ojos izquierdos, mientras que el fletán es de ojos derechos.
Véase también
- Asimetría
- Mano dominante
- Metaquiralidad
- Orientación (matemáticas)
- Regla de la mano derecha
- Sinistral y dextral
- Estereoquímica
- Perversión de zarcillo
Referencias
- ↑ Sir William Thomson Lord Kelvin (1894). The Molecular Tactics of a Crystal. Clarendon Press.
- ↑ Georges Henry Wagnière, On Chirality and the Universal Asymmetry: Reflections on Image and Mirror Image (2007).
- ↑ Petitjean, M. (2017). «Chirality in metric spaces. In memoriam Michel Deza». Optimization Letters. doi:10.1007/s11590-017-1189-7.
- ↑ «Looking for the Right Hand - DiscoverMagazine.com». discovermagazine.com. Consultado el 23 de marzo de 2018.
- ↑ a b «Quantum Diaries». www.quantumdiaries.org. Consultado el 23 de marzo de 2018.
- ↑ Organic Chemistry (4th Edition) Paula Y. Bruice.
- ↑ Organic Chemistry (3rd Edition) Marye Anne Fox, James K. Whitesell.
- ↑ Unión Internacional de Química Pura y Aplicada. «chirality». Compendium of Chemical Terminology. Versión en línea (en inglés).
- ↑ Chang, Raymond (1984). Chemistry (second edición). Random House. p. 660. ISBN 978-0-394-32983-3.
- ↑ Moloney, Mícheál P.; Gun'ko, Yurii K.; Kelly, John M. (26 de septiembre de 2007). «Chiral highly luminescent CdS quantum dots». Chemical Communications (en inglés) 0 (38): 3900-2. ISSN 1364-548X. PMID 17896026. doi:10.1039/b704636g.
- ↑ Schaaff, T. Gregory; Knight, Grady; Shafigullin, Marat N.; Borkman, Raymond F.; Whetten, Robert L. (1 de diciembre de 1998). «Isolation and Selected Properties of a 10.4 kDa Gold:Glutathione Cluster Compound». The Journal of Physical Chemistry B 102 (52): 10643-10646. ISSN 1520-6106. doi:10.1021/jp9830528.
- ↑ Ma, Wei; Xu, Liguang; de Moura, André F.; Wu, Xiaoling; Kuang, Hua; Xu, Chuanlai; Kotov, Nicholas A. (28 de junio de 2017). «Chiral Inorganic Nanostructures». Chemical Reviews 117 (12): 8041-8093. ISSN 0009-2665. PMID 28426196. doi:10.1021/acs.chemrev.6b00755.
- ↑ Xiao, Wende; Ernst, Karl-Heinz; Palotas, Krisztian; Zhang, Yuyang; Bruyer, Emilie; Peng, Lingqing; Greber, Thomas; Hofer, Werner A. et al. (8 de febrero de 2016). «Microscopic origin of chiral shape induction in achiral crystals». Nature Chemistry (en inglés) 8 (4): 326-330. ISSN 1755-4330. PMID 27001727. doi:10.1038/nchem.2449.
- ↑ Solomon and Fryhles organic chemistry, Ed 10, Wiley (Students edition), Chapter 5 (Stereochemistry), Section 5.5 More about biological significance of chirality
- ↑ Solomon and Fryhles organic chemistry, Ed 10, Wiley (Students edition), Chapter 5 (Stereochemistry), review problem 5.14
- ↑ Sanganyado, Edmond; Lu, Zhijiang; Fu, Qiuguo; Schlenk, Daniel; Gan, Jay (2017). «Chiral pharmaceuticals: A review on their environmental occurrence and fate processes». Water Research 124: 527-542. ISSN 0043-1354. doi:10.1016/j.watres.2017.08.003.
- ↑ Solomon and Fryhles organic chemistry, Ed 10, Wiley (Students edition), Chapter 5 (Stereochemistry), section 5.11(chiral drugs)
- ↑ Suzuki, Toshinari; Kosugi, Yuki; Hosaka, Mitsugu; Nishimura, Tetsuji; Nakae, Dai (8 de octubre de 2014). «Occurrence and behavior of the chiral anti-inflammatory drug naproxen in an aquatic environment». Environmental Toxicology and Chemistry (en inglés) 33 (12): 2671-2678. ISSN 0730-7268. doi:10.1002/etc.2741.
- ↑ B, Manolescu; V, Atanasiu; C, Cercasov; I, Stoian; E, Oprea; C, Buşu (15 de noviembre de 2008). «So many options but one choice: the human body prefers α-tocopherol. A matter of stereochemistry.». Journal of Medicine and Life 1 (4): 376-382. ISSN 1844-122X. PMC 5654212. PMID 20108516.
- ↑ Schilthuizen, M.; Davison, A. (2005). «The convoluted evolution of snail chirality». Naturwissenschaften 92 (11): 504-515. Bibcode:2005NW.....92..504S. PMID 16217668. doi:10.1007/s00114-05-0045-2.
- ↑ «Amphidromus perversus (Linnaeus, 1758)». www.jaxshells.org. Consultado el 23 de marzo de 2018.
Enlaces externos
- "The Handedness of the Universe", (La Quiralidad del Universo) por Roger A Hegstrom y Dilip K Kondepudi [1]


