| Óxido de trifenilfosfano | ||
|---|---|---|
 | ||
 | ||
 | ||
| General | ||
| Otros nombres | Triphenylphosphine oxide | |
| Fórmula estructural |
 | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 791-28-6[1] | |
| Número RTECS | SZ1676000 | |
| ChEBI | 36601 | |
| ChEMBL | CHEMBL482091 | |
| ChemSpider | 12549 | |
| PubChem | 13097 | |
| UNII | Z69161FKI3 | |
| Propiedades físicas | ||
| Masa molar | 278,086 g/mol | |
El óxido de trifenilfosfina (a menudo abreviado TPPO) es el compuesto organofosforado con la fórmula OP(C6H5)3, también escrito como Ph3PO o PPh3O (Ph = C6H5). Este compuesto cristalino incoloro es un producto de desecho común pero potencialmente útil en reacciones que involucran trifenilfosfina. Es un reactivo popular para inducir la cristalización de compuestos químicos.
YouTube Encyclopedic
-
1/3Views:17 32353 8611 787
-
Mecanismo de la reacción de Wittig. Preparación del iluro de fósforo
-
Oxidación de Alcoholes | Obtención de Ácidos Carboxílicos, Aldehídos y Cetonas
-
QUIMICA Que es la Energía de Estabilización Campo Cristalino TCC AULAEXPRESS
Transcription
Estructura y propiedades
Ph3PO es una molécula tetraédrica relacionada con POCl3. El centro de oxígeno es relativamente básico. La rigidez de la columna vertebral y la basicidad del centro de oxígeno hacen de esta especie un agente popular para la cristalización de moléculas que de otro modo serían difíciles de cristalizar. Este truco es aplicable a moléculas que tienen átomos de hidrógeno ácidos, p. ej. fenoles.[2][3]
Hasta ahora, se han encontrado varias modificaciones de Ph3PO. Por ejemplo, una forma monoclínica cristaliza en el grupo espacial P21/c con Z = 4 y a = 15.066(1) Å, b = 9.037(2) Å, c = 11.296(3) Å, y β = 98,47(1) Å. La modificación ortorrómbica cristaliza en el grupo espacial Pbca con Z = 4 y 29.089(3) Å, b = 9.1347(9), c = 11.261(1) Å.[4][5]
Como subproducto de síntesis orgánica
Ph3PO es un subproducto de muchas reacciones útiles en la síntesis orgánica, incluidas las reacciones de Wittig, Staudinger y Mitsunobu. También se genera cuando se emplea PPh3Cl2 para convertir alcoholes en cloruros de alquilo:
- Ph3PCl2 + ROH → Ph3PO + HCl + RCl
La trifenilfosfina se puede regenerar a partir del óxido mediante el tratamiento con una variedad de agentes desoxigenantes, como fosgeno o triclorosilano/trietilamina:[6]
- Ph3PO + SiHCl3 → PPh3 + 1/n (OSiCl2)n + HCl
El óxido de trifenilfosfina puede ser difícil de eliminar de las mezclas de reacción mediante cromatografía. Es poco soluble en hexano y en éter dietílico frío. A menudo, la trituración o la cromatografía de productos «en bruto» (impuros) con estos disolventes conduce a una buena separación del óxido de trifenilfosfina. Su eliminación se facilita mediante la conversión a su complejo de Mg (II), que es poco soluble en tolueno o en diclorometano y se puede filtrar. Puede usarse un método de filtración alternativo en el que se genera ZnCl2(TPPO)2 tras la adición de ZnCl2 con disolventes más polares como etanol, acetato de etilo y tetrahidrofurano.[7][8]
Química de coordinación
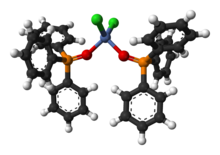
Ph3PO es un ligando para centros metálicos «duros». Un complejo representativo es la especie tetraédrica NiCl2(OPPh3)2.[9]
Ph3PO es una impureza común en PPh3. La oxidación de PPh3 por oxígeno, incluyendo aire, es catalizada por muchos iones de metal:
- 2 PPh3 + O2 → 2 Ph3PO
Referencias
- ↑ Número CAS
- ↑ D. E. C. Corbridge "Phosphorus: An Outline of its Chemistry, Biochemistry, and Technology" 5th Edition Elsevier: Amsterdam. ISBN 0-444-89307-5.
- ↑ M. C. Etter and P. W. Baures (1988). «Triphenylphosphine oxide as a crystallization aid». J. Am. Chem. Soc. 110 (2): 639-640. doi:10.1021/ja00210a076.
- ↑ Spek, Anthony L. (1987). «Structure of a second monoclinic polymorph of triphenylphosphine oxide». Acta Crystallographica. C43: 1233-1235. doi:10.1107/S0108270187092345.
- ↑ Al-Farhan, Khalid A. (1992). «Crystal structure of triphenylphosphine oxide». Journal of Crystallographic and Spectroscopic Research 22 (6): 687-689. doi:10.1007/BF01160986.
- ↑ van Kalkeren, H. A.; van Delft, F. L.; Rutjes, F. P. J. T. (2013). «Organophosphorus Catalysis to Bypass Phosphine Oxide Waste». ChemSusChem 6: 1615-1624. doi:10.1002/cssc.201300368.
- ↑ Patent WO 1998007724. "Process for the preparation of 7-alkoxyalkyl-1,2,4-triazolo[1,5-a] pyrimidine derivatives"
- ↑ Batesky, Donald C.; Goldfogel, Matthew J.; Weix, Daniel J. (2017). «Removal of Triphenylphosphine Oxide by Precipitation with Zinc Chloride in Polar Solvents». The Journal of Organic Chemistry (en inglés) 82 (19): 9931-9936. doi:10.1021/acs.joc.7b00459.
- ↑ D. M. L. Goodgame and M. Goodgame (1965). «Near-Infrared Spectra of Some Pseudotetrahedral Complexes of Cobalt (II) and Nickel(II)». Inorg. Chem. 4 (2): 139-143. doi:10.1021/ic50024a002.
Enlaces externos
- Esta obra contiene una traducción derivada de «Triphenylphophine oxide» de Wikipedia en inglés, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.
