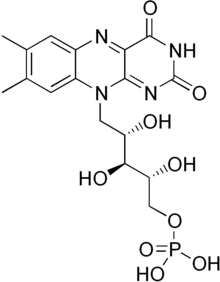
Флавины (лат. flavus — жёлтый) — группа органических соединений - производных диметилизоаллоксазина ((7,8-диметилбензо[g]птеридин-2,4(3H,10H)-диона)), замещенных обычно по положению 10[1].
Флавины широко распространены в живых организмах, основными представителями флавинов являются: На основе молекулы флавина (гетероциклического изоаллоксазина) построены молекулы ключевых коферментов клетки:
- Рибофлавин (витамин В2) - 10-рибофлавин
- FMN, флавинмононуклеотид - фосфорилированный по концевому гидроксилу рибозного остатка рибофлавин (рибофлавин-5'-фосфат)
- FAD, флавинадениндинуклеотид - динуклеотид аденозина и рибофлавинна
Свойства
Флавины способны к обратимому восстановлению, принимая два электрона и образуя восстановленную дигидроформу:
Окисление-восстановление флавинов идет в две стадии - с образованием при одноэлектронном окислении-восстановлении ион-радикальной семихинонной формы, что обуславливает участие флавинов в биохимических процессах окисления как по нуклеофильному, так и по радикальному механизмам:
Флавины окрашены в желтый цвет и способны к флуоресценции. Так, рибофлавин имеет максимум поглощения в синей области (λmax ~450 нм) и флуоресцирует в желто-зеленой области (λmax ~565 нм).
Биологическое значение
Способность к обратимому восстановлению флавинов обуславливает тот факт, что они являются коферментами множества ферментов-оксидоредуктаз - дегидрогеназ, оксидаз и монооксигеназ в том числе и ферментов дыхательной цепи переноса электронов, в последнем случае флавиновые оксилоредуктазы являются частью редокс-цепи окисления-восстановления никотинамидадениндинуклеотида (НАД) или его фосфата (НАДФ):
флавин + НАДФ-Н + H+ восстановленный флавин + NADP + H+
Флавиновые ферменты катализируют окисление связей как углерод-углерод (например, сукцинатдегидрогеназа, катализиирующая окисление янтарной кислоты в цикле трикарбоновых кислот, ферменты окислительного декарбоксилирования пировиноградной и a-кетоглутаровой кислот), так и связей углерод-гетероатом.
К группе флавиновых ферментов, окисляющих связь углерод-азот, относятся ферменты метаболизма аминов и их производных - моноаминооксидазы, оксидазы D-аминокислот, ксантиноксидазы, катализирующие окисление пуринов в конечный продукт их метаболизма - мочевую кислоту и ряд других групп ферментов.
К флавиновым ферментам, окисляющим связь углерод-кислород, относятся альдегидоксидазы, окисляющие высокотоксичные альдегиды (в том числе и получающиеся окислением спиртов алкогольдегидрогеназами) до карбоновых кислот и некоторые ферменты, окисляющие сахара - например, глюкозооксидаза, окисляющая глюкозу до глюконовой кислоты.
Флавинсодержащая глутатионредуктаза катализирует восстанавление дисульфидной связи окисленного глутатиона GSSG до его сульфгидрильной формы GSH, роль восстановителя в этой реакции играет НАДФ-Н.
Примечания
- ↑ flavins // IUPAC Gold Book. Дата обращения: 20 августа 2020. Архивировано 23 января 2021 года.
Ссылки
- [www.xumuk.ru/encyklopedia/2684.html Флавин | Химическая энциклопедия].
Обычно почти сразу, изредка в течении часа.




